В ЄС рекомендували препарат для лікування COVID-19
Київ • УНН
КИЇВ. 26 червня. УНН. Європейське агентство з лікарських засобів (EMA) у четвер, 25 червня, рекомендувало схвалити препарат ремдесивір як ліки проти COVID-19. Це перший препарат, що отримав дозвіл на використання від ЕМА, зазначається на сайті агентства, передає УНН із посиланням на DW.
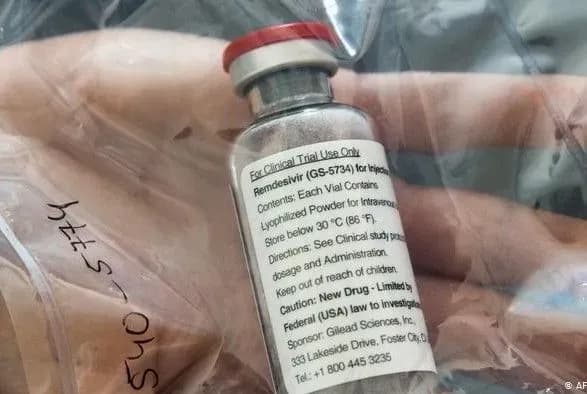
“Дані про ремдесівір були оцінені у винятково короткі строки за допомогою особливої процедури, що використовується ЕМА під час надзвичайних ситуацій в галузі охорони здоров’я для оцінки даних в міру того, як вони надходять”, — йдеться в заяві.
За результатами оцінки препарату надана рекомендація, заснована в основному на даних дослідження NIAID-ACTT-11, що спонсорується Націнститутом алергії та інфекційних захворювань США (NIAID), а також на даних інших досліджень ремдесивіра.
У дослідженні NIAID-ACTT-1 оцінювалася ефективність 10-денного курсу лікування ремдесивіром у понад 1000 пацієнтів, госпіталізованих з COVID-19. Ремдесивір порівнювали з плацебо (фіктивне лікування), і основним показником ефективності був час одужання пацієнтів.
ЧИТАЙТЕ ТАКОЖ: Зеленський дозволив продовжити застосування експериментальних препаратів для лікування COVID-19
У цілому дослідження показало, що пацієнти, які отримували ремдесівір, одужували приблизно через 11 днів, у порівнянні з 15 днями для пацієнтів, які отримували плацебо. Цей ефект не спостерігався у пацієнтів з легким та середнім ступенем тяжкості захворювання: час до одужання становив 5 днів як для групи ремдесівіру, так і для групи плацебо. Для пацієнтів з важким перебігом хвороби, які становили приблизно 90 відсотків досліджуваної групи, час до одужання становив 12 днів у групі ремдесівіру та 18 днів у групі плацебо.
Згідно з рекомендацією, препарат має бути схвалений для лікування COVID-19 у дорослих і підлітків віком від 12 років, які мають пневмонію і які потребують додаткового кисню.
ЧИТАЙТЕ ТАКОЖ: Пандемія: Китай схвалив проведення клінічних випробувань шостої вакцини проти COVID-19
Ця рекомендація потребує схвалення у Єврокомісії, яка має ухвалити рішення наступного тижня.
Як повідомлялося, управління з санітарного нагляду за якістю продовольства та медикаментів міністерства охорони здоров’я США (FDA)видало екстрений дозвіл на використання у виняткових випадках препарату ремдесивір у лікарнях пацієнтами з атиповою пневмонією COVID-19 ще на початку травня.
Ремдесивір був розроблений американською біотехнологічною компанією Gilead Sciences для боротьби з лихоманкою Ебола, а пізніше показав ефективність у боротьбі зі збудниками коронавірусів SARS і MERS.
ЧИТАЙТЕ ТАКОЖ: Трамп розповів, який препарат він приймає для захисту від коронавірусу